Bruce e il mito dell’alfa. La storia del kea senza becco che ha vinto tutte le battaglie, e perché quella parola non spiega nulla di ciò che è successo davvero
Nel 2013 un ricercatore trova un giovane kea ferito nell’Arthur’s Pass National Park, sulle Alpi meridionali della Nuova Zelanda.
L’uccello è vivo, ma la parte superiore del becco non c’è più, è stata amputata, con ogni probabilità, da una trappola per ratti.
Lo raccolgono, lo portano alla Willowbank Wildlife Reserve di Christchurch, gli danno un nome: Bruce.
Negli anni successivi Bruce impara a mangiare premendo il cibo contro oggetti duri, a compensare quello che manca con ciò che resta.
Nel 2019 i keeper della riserva iniziano a osservare qualcosa di insolito:
Bruce raccoglie sistematicamente piccoli sassolini da terra e li usa per pulire le proprie penne.
Nel 2021 uno studio pubblicato su Scientific Reports documenta per la prima volta un pappagallo che usa strumenti per la cura di sé.
Bruce seleziona i sassi per dimensione, li muove tra lingua e mandibola, li sostituisce quando non sono adatti.
È un comportamento intenzionale, innovativo, assente negli altri dodici kea della stessa voliera.
Nel 2026, cinque anni dopo, un nuovo studio pubblicato su Current Biology da Grabham e colleghi dell’Università di Canterbury documenta il capitolo successivo della storia di Bruce:
in quattro settimane di osservazione sistematica, Bruce ha vinto tutte le interazioni agonistiche con gli altri maschi del gruppo, trentasei su trentasei.
È il primo ad accedere al feeder l’ottantatré per cento dei giorni.
Ha i livelli di metaboliti del corticosterone più bassi di tutti. È l’unico maschio a ricevere allopreening da individui non-partner.
I titoli di mezzo mondo lo hanno definito l’“alfa” del suo gruppo. “Alfa” è una parola immediata, riconoscibile, che funziona bene nei comunicati stampa, ma è anche una parola che dice poco di quello che è successo e che rischia di oscurare le parti più interessanti della storia.
Prima di tutto: chi sono i kea
Nestor notabilis è l’unico pappagallo alpino al mondo.
Vive tra i 1.200 e i 2.000 metri sulle Alpi meridionali della Nuova Zelanda, in un habitat di rocce, faggio antartico e correnti d’aria fredda.
È onnivoro, opportunista, generalista in senso ecologico profondo: d’estate segue i fiori e i frutti, d’inverno scende di quota, non disdegna carogne, tuberi, invertebrati e, fatto che gli costò la persecuzione umana per decenni, la carne viva delle pecore, attaccandone il grasso della schiena. Non generalizzate a tutti i pappagalli questa peculiarità!
La specie è in pericolo: si stima che ne rimangano tra i 3.000 e i 7.000 individui.
Ma ciò che rende il kea rilevante per questa storia non è la sua dieta. È il suo cervello.
Nel 2016 una ricerca pubblicata su PNAS da Olkowicz e colleghi ha misurato la densità neuronale nel proencefalo di 28 specie aviarie, così i risultati hanno costretto a riscrivere alcune assunzioni di base sulla cognizione degli uccelli:
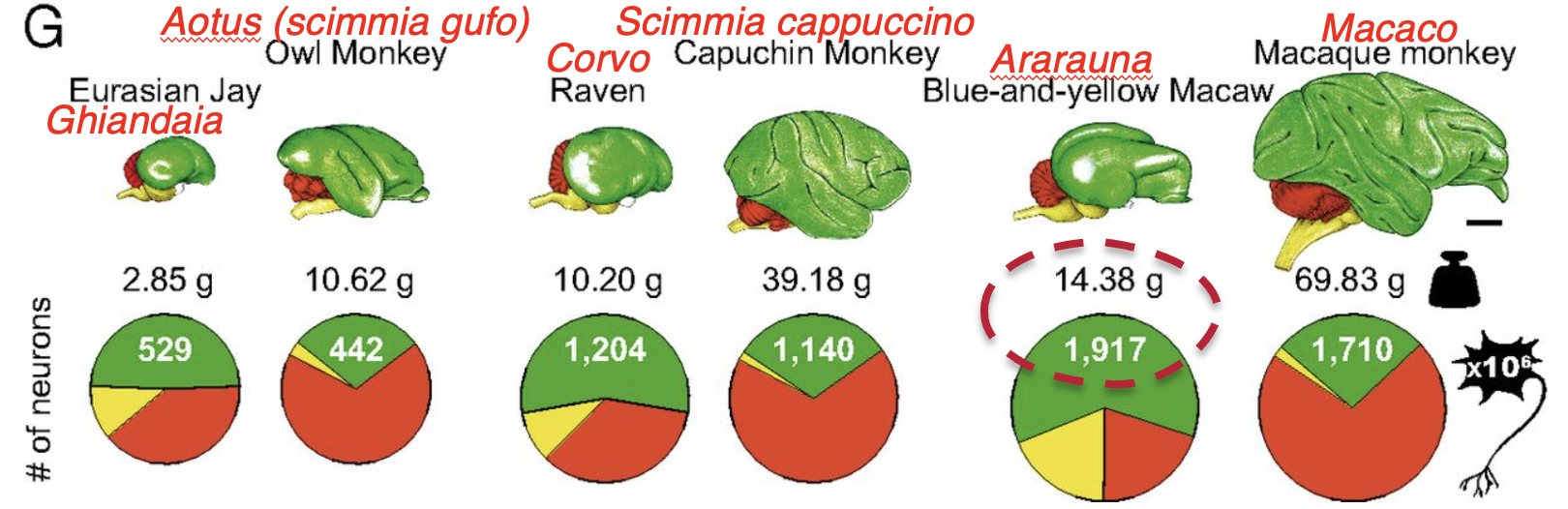
i pappagalli e i corvidi hanno in media il doppio dei neuroni dei primati a parità di massa cerebrale.
Un’Ara blu-e-gialla ha circa 1,9 miliardi di neuroni palliali — paragonabili a un macaco. Il kea è tra le specie con i valori più alti.
Quella densità neuronale non è un casuale evento anatomico. È il prodotto di una pressione evolutiva specifica: un’ontogenesi lunga, un periodo di dipendenza parentale prolungato, una finestra di apprendimento sociale estesa nel tempo.
I giovani kea rimangono associati ai genitori ben oltre la capacità tecnica di sopravvivere da soli, continuando a osservare, a imitare, a esplorare sotto la protezione del gruppo familiare. È questa infanzia prolungata che ha reso possibile il cervello. E è quel cervello che rende possibile la storia di Bruce.
Una società fluida: cosa significa davvero
I kea non vivono in branchi stabili con gerarchie fisse. Vivono in aggregazioni temporanee che si formano e si dissolvono in funzione delle risorse disponibili, della stagione e degli individui presenti in un dato momento.
Il termine tecnico è fission-fusion: il gruppo si divide e si ricostituisce continuamente, e la sua composizione non è mai garantita da un giorno all’altro.
Presso le discariche e le stazioni sciistiche (dove le concentrazioni di kea sono state studiate più sistematicamente) i ricercatori Judy Diamond e Alan Bond hanno descritto aggregazioni fino a quaranta individui composte da unità familiari, coppie riproduttive e gruppi di subadulti maschi non riproduttivi che si mescolano in proporzioni variabili.
Solo la coppia che nidifica e i piccoli dell’anno formano un nucleo stabile nel tempo. Tutto il resto è in movimento.
In questa struttura, le relazioni di dominanza non seguono una gerarchia lineare.
Tebbich, Taborsky e Winkler nel 1996 documentarono che il kea A può dominare B, B può dominare C, ma C può dominare A.
Una catena circolare, non una piramide.
Gli stessi dati dello studio Grabham del 2026 lo confermano: l’indice di linearità della gerarchia del gruppo di Bruce è statisticamente non significativo. Il gruppo non ha una gerarchia stabile, o meglio, ne ha una solo perché è un gruppo captivo chiuso da anni.
E qui sta il primo problema con la parola “alfa”.
La parola sbagliata e la storia del suo errore
Il concetto di “maschio alfa” nelle società animali nasce da uno studio del 1947 di Rudolf Schenkel su lupi tenuti in cattività in uno zoo di Basilea.
Quegli animali non erano imparentati tra loro, erano stati messi insieme artificialmente, e le interazioni agonistiche frequenti che Schenkel osservò erano il prodotto diretto di quella forzatura ambientale.
Il concetto di “maschio alfa” (l’individuo che domina con la forza e mantiene il controllo tramite intimidazione) fu costruito su quelle osservazioni e poi applicato ad altre specie, inclusa la nostra.
L’ironia della storia è che il più noto divulgatore di quel concetto ha poi chiesto pubblicamente che venisse ritrattato: L. David Mech.
Così, nel 1999 L. David Mech, il ricercatore che più di chiunque altro aveva diffuso la nozione di “lupo alfa”, pubblica su Canadian Journal of Zoology un articolo in cui smonta la sua stessa opera.
Onore al suo lavoro e onore alla sua onestà intellettuale, comportamento così poco comune nello scientismo e invece fiammella viva nella scienza.
I branchi di lupi selvatici, scrive, non sono gruppi di individui non imparentati in competizione per il rango: sono famiglie.
I genitori guidano i figli non perché li dominano, ma perché li hanno generati e li conoscono.
Il maschio dominante è semplicemente il padre.
Mech ha poi contattato il suo editore chiedendo di cessare le ristampe del libro del 1970 in cui aveva reso popolare il termine.
Nei primati la situazione è più sfumata, ma Frans de Waal ha dedicato decenni a documentare come la leadership negli scimpanzei dipenda da alleanze, comportamenti affiliativi, grooming e capacità di mediazione dei conflitti, non dalla forza bruta.
Il maschio che chiamiamo “alfa”, è spesso quello che consolida le coalizioni, non quello che spaventa gli altri.
Per i kea, il concetto di “maschio alfa” è ancora meno applicabile.
In una società dove le relazioni di dominanza sono intransitive, dove il gruppo si ricostituisce stagionalmente, dove la stragrande maggioranza dei maschi non si riproduce in un dato anno senza che questo costituisca una patologia sociale, e dove la coesione è mantenuta dal gioco e dall’affiliazione più che dalla gerarchia, chi sarebbe l’alfa? A quale titolo? Per quanto tempo? …
Gli stessi autori dello studio di Grabham lo riconoscono esplicitamente nel testo: i kea selvatici hanno dinamiche sociali “much more fluid and complicated”, e i kea in cattività sono soggetti a gerarchie più rigide proprio perché la composizione del gruppo è fissa.
Il titolo dello studio “A disabled kea parrot is the alpha male of his circus” usa il termine come descrittore operativo di un fenomeno captivo, non come tesi sulla specie.
La parola “alfa” è entrata nei titoli dei giornali perché è immediata e universalmente riconoscibile…come gli errori concettuali prendono radice e diventano faticosi da elidere.
Questo termine dunque, semplifica fino all’erroneo. E oscura la cosa davvero straordinaria che è accaduta a Bruce.
Ciò che Bruce ha fatto davvero
Nel gruppo di Willowbank ci sono dodici individui.
Nove maschi, tre femmine.
Bruce è uno dei maschi adulti, e a differenza di tutti gli altri non ha la rinoteca*.
Nota*:
Rinoteca
È solo la porzione superiore del rivestimento corneo del becco degli uccelli. E’ la parte superiore del becco.
Ranfoteca
È il rivestimento corneo completo del becco, quindi comprende: rinoteca (parte superiore) e gnatoteca (parte inferiore).
Il becco del kea è un organo complesso: la parte superiore è lunga, curva, appuntita, e viene usata, tra le altre cose, come arma nelle interazioni agonistiche tra maschi.
La sequenza tipica di uno scontro prevede che il maschio sino a quel momento più forte attacchi dall’alto verso il basso, usando il becco superiore per spingere l’avversario.
Bruce non può fare questo. Non ha la struttura anatomica che lo renderebbe possibile. Quello che fa invece è spingere in avanti la mandibola inferiore esposta, usandola come un’arma da punta in una tecnica che i ricercatori hanno chiamato beak jousting, giostra del becco.
Il tasso di successo di questa tecnica è del 73%, contro il 48% dei colpi usati dagli altri maschi nelle stesse interazioni.
È una tecnica che nessun altro kea del gruppo può fisicamente replicare, perché nessun altro ha la mandibola superiore mancante!
Bruce ha quindi trasformato la sua disabilità in un vantaggio agonistico unico.
Non imitando gli altri, non facendosi aiutare da alleati poichè nessuno lo ha supportato in nessuno degli scontri documentati, ma inventando una soluzione che non esisteva nel repertorio della specie.
È innovazione comportamentale in senso stretto: una nuova soluzione a un nuovo problema, stabilizzata attraverso l’esperienza.
Questo è il dato scientificamente rilevante. Non che Bruce sia “alfa”, ma che sia arrivato dove è arrivato attraverso la plastica cognizione che caratterizza i kea, applicata a un dominio (quello della competizione sociale) in cui di solito si studia l’intelligenza solo come sottoprodotto di altri comportamenti.
I dati che i titoli non hanno riportato
Lo studio di Grabham documenta qualcosa che vale la pena leggere con attenzione, perché contraddice alcune intuizioni immediate sulla dominanza e sul benessere.
Si parla di Motivazione*, qualcosa che sgorga “da dentro” l’organismo scritto indelebilmente nei geni di specie da non confondere con l’incentivo (più sotto nella Nota*)
Bruce ha i livelli di metaboliti glucocorticoidi* fecali più bassi dell’intero gruppo.
(Nota*: FGM - Fecal Glucocorticoid Metabolites,sono utilizzati come indicatore non invasivo per monitorare lo stress fisiologico negli uccelli)
Il maschio più stressato è Taz, che è anche quello che pulisce Bruce con maggiore frequenza all’interno della mandibola inferiore esposta (la zona dove Bruce, fisicamente, non può raggiungersi da solo).
Megatron, Joker e Neo lo fanno con frequenza minore ma con costanza.
Bruce è l’unico maschio del gruppo a ricevere questo comportamento affiliativo da individui che non sono il suo partner.
Nota* e richiamo sulla Motivazione: un termine di cui è facile approfittare e che va chiarito
La differenza riguarda l’origine della motivazione e, per conseguenza, il termine usato deve cambiare:
Incentivo - ambiente esterno - per es: vista/odore del cibo
Motivazione - bisogno interiore - per es: motivazione affiliativa (bisogno di appartenenza al gruppo sociale)
Questo è insolito. Nei pappagalli, come nei primati, l’allopreening è un comportamento riservato alle relazioni preferenziali.
Non si puliscono le penne di chiunque: si puliscono quelle di chi si conosce bene, di chi ci si fida, di chi ha qualcosa da offrire in cambio.
Morales Picard e colleghi nel 2020 hanno mostrato che nei pappagalli e nei corvidi l’allopreening è predetto dalla vicinanza spaziale e dal valore relazionale del partner, con la pulizia della testa riservata ai legami più profondi.
Gli autori dello studio interpretano questo pattern come correlato al rango dominante di Bruce: gli altri si avvicinano a lui perché è il dominante, e quello che succede vicino al dominante tende ad essere affiliativo per mantenere la relazione. È una lettura plausibile. C’è però anche un’altra lettura possibile, non necessariamente alternativa: Bruce ha una zona del corpo inaccessibile a sé stesso e vitalmente importante per la salute del piumaggio. Il fatto che altri individui la puliscano con frequenza potrebbe riflettere anche una funzione compensatoria reale, non solo un’affiliazione indotta dal rango.
Non sappiamo quale delle due letture sia corretta, o in che misura convivano. Lo studio non era progettato per rispondere a questa domanda. Ma il pattern è là, nei dati, e merita di essere nominato.
La società che si tiene insieme col gioco
Per capire perché il rango di Bruce non equivale a un alfa, bisogna capire come i kea costruiscono la coesione sociale in assenza di gerarchie stabili.
I kea giocano. Lo fanno a tutte le età, con intensità e varietà che non hanno paragoni tra gli uccelli.
Giocano da soli con oggetti, giocano in coppia inseguendosi, giocano in gruppo in combattimenti ritualizzati che coinvolgono piume arruffate, vocalizzazioni specifiche e sequenze stereotipate che non hanno nulla a che fare con l’aggressione reale.
Diamond e Bond, che hanno studiato i kea per più di trent’anni, descrivono il gioco come il principale meccanismo di apprendimento sociale della specie e il mastice che tiene insieme aggregazioni di individui che altrimenti non avrebbero ragione di stare vicini.
Nel 2017 Raoul Schwing e colleghi hanno pubblicato su Current Biology uno studio che ha cambiato la comprensione del gioco aviare.
Tramite playback ad Arthur’s Pass, hanno dimostrato che la “play call” del kea (un warble - gorgheggio - acuto che gli individui emettono mentre giocano) induce spontaneamente comportamenti di gioco anche in individui che non stavano giocando e che si trovavano nelle vicinanze senza interazione diretta.
È contagio emotivo: l’equivalente funzionale della risata umana, primo caso documentato in un non-mammifero.
Questa scoperta non è solo curiosa.
Ha un’implicazione strutturale: in una specie dove le emozioni positive si propagano attraverso vocalizzazioni, la coesione del gruppo non dipende dalla paura dell’individuo dominante.
Dipende dall’attrazione reciproca, dalla piacevolezza dell’interazione, dalla motivazione di stare vicini perché stare vicini è funzionalmente gratificante.
In questo contesto, la dominanza di Bruce funziona in modo diverso da quella di un lupo alfa classico descritto nella “prima-maniera” di L. David Mech.
Bruce non tiene insieme il gruppo. Non ha alleati su cui si appoggia.
Non consolida la sua posizione attraverso grooming strategico.
Vince gli scontri fisici quando si verificano, usando una tecnica che gli altri non possono replicare.
Questo gli garantisce accesso prioritario al cibo e bassa risposta allo stress, ma il gruppo (la sua struttura, la sua coesione, i suoi affetti) esiste indipendentemente da Bruce, regolato da meccanismi che il rango agonistico non esaurisce.
Quando il dominante sa farsi da parte
C’è un altro elemento della socialità dei kea che complica ulteriormente la presunta cornice dell’alfa: la cooperazione funziona meglio quando il dominante si trattiene.
Schwing, Jocteur, Wein, Noë e Massen nel 2016 hanno testato coppie di kea nel paradigma della “loose-string” ( = della corda allentata): per ottenere cibo, entrambi gli individui devono tirare simultaneamente un’estremità di una corda.
Il risultato più rilevante non è che i kea cooperano, questo lo sapevamo già, ma che cooperano di più con partner affiliati e, crucialmente, che la cooperazione nei gruppi con un dominante presente funziona solo quando il dominante si trattiene dall’accaparrarsi il cibo al momento della ricompensa.
Un dominante che rispetta il contributo dell’altro abilita la cooperazione. Un dominante che sfrutta il partner la interrompe.
Questo risultato è stato poi esteso a cooperazioni a tre e quattro individui (la prima cooperazione tetradica documentata in un non-umano) confermando lo stesso pattern.
La struttura sociale dei kea non si basa sul controllo del dominante, ma sulla tolleranza del dominante. È una distinzione che cambia tutto nella comprensione di come funziona la leadership in questa specie.
Bruce, nei quattro anni in cui è stato osservato alla Willowbank, non ha dati pubblicati sulla sua partecipazione a task cooperativi. Ma i dati del 2026 mostrano che i suoi livelli di stress sono bassi e che riceve affiliazione.
Un individuo ad alto stress che impone la propria posizione tramite intimidazione continua, tenderebbe a pattern opposti.
Il fatto che Bruce mantenga la posizione agonistica con bassa attivazione cronica del sistema dello stress suggerisce che la sua dominanza non è costantemente contestata e non richiede vigilanza continua, un profilo diverso da quello di un dominante che deve difendersi da sfidanti in una gerarchia instabile.
Il confronto che la letteratura non aveva ancora visto
Prima di Bruce, la letteratura sulla disabilità e lo status sociale negli animali cognitivamente complessi aveva un unico caso di riferimento: Faben, uno scimpanzé maschio del gruppo di Gombe colpito da polio nel 1966.
Faben perse quasi del tutto l’uso del braccio sinistro. Jane Goodall lo osservò per anni. Faben raggiunse il rango beta nel gruppo (non l’alfa, il secondo) ma lo fece grazie a un fattore fondamentale: l’alleanza con suo fratello Figan, che sarebbe diventato il maschio alfa del gruppo.
Il caso di Bruce è strutturalmente diverso:
Bruce non ha fratelli nel gruppo. Non ha alleati documentati.
Ha raggiunto e mantenuto la posizione agonistica più alta “in solitaria”, con il supporto di nessun altro individuo, tramite un’innovazione comportamentale che ha sviluppato autonomamente.
Questo è il dato che gli autori considerano inedito nella letteratura. Non tanto il risultato in sé (un pappagallo disabile che vince gli scontri) ma la via con cui ci è arrivato.
Il modello precedente prevedeva che un disabile ad alto rango dovesse compensare il deficit fisico con risorse sociali: alleanze, coalizioni, supporto.
Bruce ha compensato il deficit fisico con un’innovazione tecnica. Ha usato il cervello in senso letterale, inventando una soluzione che sfrutta la sua morfologia alterata invece di aggirarla.
Christina Riehl di Princeton, commentando lo studio, ha avvertito che conclusioni ampie non dovrebbero essere tratte da un singolo individuo in cattività. Ha ragione. Bruce è un caso, non una regola. Ma è un caso che occupa un posto unico nella letteratura, e che apre domande precise: in quali condizioni un animale cognitivamente complesso può compensare un deficit fisico con innovazione comportamentale? La risposta dipende dal cervello, dalla società in cui vive, o da entrambi?
Ciò che la parola “alfa” non riesce a contenere
Bruce è un kea senza la metà del becco che ha vinto tutte le battaglie del suo gruppo usando una tecnica che ha inventato da solo. Questo è un fatto straordinario, ed è straordinario con o senza la parola “alfa”.
Il problema di quella parola, Alfa, non è che sia falsa in senso tecnico stretto: Bruce è l’individuo con la posizione agonistica più alta nel suo gruppo.
Il problema è che porta con sé un bagaglio di implicazioni che non si applicano.
Implica una gerarchia lineare stabile: i kea non ce l’hanno, o ce l’hanno solo in cattività.
Implica che la posizione sia mantenuta tramite intimidazione: Bruce la mantiene tramite una tecnica di combattimento, non tramite segnali continui di dominanza.
Implica che il gruppo sia organizzato intorno alla volontà dell’individuo dominante: la società dei kea è organizzata intorno al gioco, all’affiliazione, alla cooperazione e alla tolleranza.
Chiamarlo “alfa” semplifica Bruce fino a renderlo irriconoscibile.
La versione vera è molto più interessante: Bruce è un individuo che ha perso una struttura anatomica fondamentale per la sua specie, ha trascorso anni a imparare a mangiare e a pulirsi con ciò che gli restava, e poi ha trasformato il suo stesso deficit in uno strumento di vantaggio in un dominio completamente diverso.
L’ha fatto in una specie dove la flessibilità cognitiva è il tratto più selezionato, dentro una società dove la tolleranza è il tessuto connettivo.
Non è la storia di un alfa. È la storia di un cervello che non si ferma davanti a un problema che non ha soluzione standard. Ed è anche, in modo più sottile, la storia di un gruppo che gli ha permesso di arrivarci.
─────────────────────────────────────────
Riferimenti scientifici
Lo studio originale e la ricerca su Bruce
Grabham A.A. et al. (2026). A disabled kea parrot is the alpha male of his circus. Current Biology. DOI: 10.1016/j.cub.2026.03.004.
Bastos A.P.M. et al. (2021). Self-care tooling innovation in a disabled kea (Nestor notabilis). Scientific Reports, 11: 18035. DOI: 10.1038/s41598-021-97086-w.
Struttura sociale e cognizione dei kea
Tebbich S., Taborsky M. & Winkler H. (1996). Social manipulation causes cooperation in keas. Animal Behaviour, 52(1): 1–10.
Diamond J. & Bond A.B. (1991). Social behavior and the ontogeny of foraging in the kea (Nestor notabilis). Ethology, 88(2): 128–144.
Diamond J. & Bond A.B. (1999). Kea, Bird of Paradox: The Evolution and Behavior of a New Zealand Parrot. University of California Press.
Diamond J. & Bond A.B. (2003). A comparative analysis of social play in birds. Behaviour, 140(8): 1091–1115.
Schwing R., Jocteur E., Wein A., Noë R. & Massen J.J.M. (2016). Kea cooperate better with sharing affiliates. Animal Cognition, 19: 1093–1102.
Schwing R., Nelson X.J., Wein A. & Parsons S. (2017). Positive emotional contagion in a New Zealand parrot. Current Biology, 27(6): R213–R214.
Schwing R., Meaux E., Piseddu A., Huber L. & Noë R. (2021). Kea, Nestor notabilis, achieve cooperation in dyads, triads, and tetrads when dominants show restraint. Learning & Behavior, 49: 158–173.
Neurobiologia aviare
Olkowicz S. et al. (2016). Birds have primate-like numbers of neurons in the forebrain. PNAS, 113(26): 7255–7260.
Uomini N., Fairlie J., Gray R.D. & Griesser M. (2020). Extended parenting and the evolution of cognition. Philosophical Transactions of the Royal Society B, 375(1803): 20190495.
Il concetto di dominanza e il mito dell’alfa
Schenkel R. (1947). Ausdrucks-Studien an Wölfen. Behaviour, 1(2): 81–129.
Mech L.D. (1999). Alpha status, dominance, and division of labor in wolf packs. Canadian Journal of Zoology, 77(8): 1196–1203.
de Waal F.B.M. (1982). Chimpanzee Politics: Power and Sex among Apes. Jonathan Cape, London.
Allopreening e comportamento affiliativo
Morales Picard A. et al. (2020). Why preen others? Predictors of allopreening in parrots and corvids and comparisons to grooming in great apes. Ethology, 126: 207–228.
Disabilità e rango sociale nei primati
Goodall J. (1986). The Chimpanzees of Gombe: Patterns of Behavior. Harvard University Press.
Morbeck M.E., Galloway A. & Zihlman A.L. (1991). The Evolving Female: A Life History Perspective. Princeton University Press.
─────────────────────────────────────────
© Parrotsmania.eu — Contenuto protetto dal diritto d’autore. Riproduzione non autorizzata vietata.